
정부가 혁신형 제약기업 인증 기준을 손질해 연구개발(R&D) 투자 비중을 높이고, 리베이트 인증기준과 심사 절차도 개선한다.
보건복지부는 26일부터 오는 5월 6일까지 '제약산업 육성 및 지원에 관한 특별법'(제약산업법) 시행령·시행규칙과 관련 고시('혁신형 제약기업 인증 등에 관한 규정') 개정안을 입법·행정예고한다고 밝혔다.
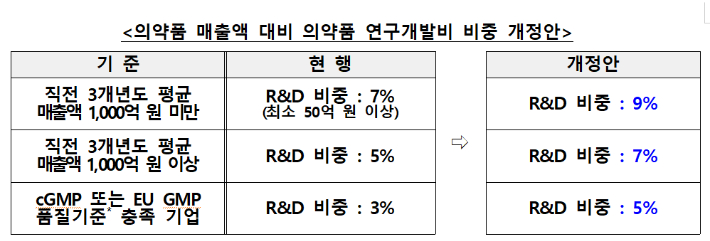
핵심 변화는 의약품 매출액 대비 의약품 R&D비 비중 기준 상향이다. 직전 3개년도 평균 매출액 1천억 원 미만 기업은 현행 7%에서 9%로, 1천억 원 이상 기업은 5%에서 7%로, cGMP·EU GMP 품질기준 충족 기업은 3%에서 5%로 각각 2%p씩 올린다.
다만 기업의 준비 기간을 고려해 시행일로부터 3년간 적용을 유예한다.
2012년 혁신형 제약기업 인증제 도입 이후 2023년까지 국내 상장 제약사의 R&D 비중은 1.4%p 오르는 데 그친 반면, 혁신형 제약기업은 3%p 상승한 점을 반영한 조치다.
 복지부 제공
복지부 제공
개정안에서는 인증 심사 시점 기준 5년 이전에 종료된 리베이트 위반행위는 심사 대상에서 제외한다. 행정심판이나 소송이 제기된 경우 기각 판결이 있는 날로부터 1년 이내에 인증을 취소할 수 있도록 했다.
그동안 오래전에 발생한 리베이트 위반으로 인해 인증이 취소되는 사례가 생기면서 기업의 예측가능성과 법적 안정성이 떨어진다는 지적에 따른 것이다.
인증 세부평가 기준도 개선된다. 심사 총점을 120점에서 100점으로 조정하고, 심사항목은 25개에서 17개로 줄인다. R&D 투자·임상시험 건수·수출 규모 등 4개 항목은 정량지표로 전환해 객관성을 높인다. 인증 최저점수(65점)는 고시에 명시하고, 탈락 기업에는 미인증 사유를 통보한다.
혁신형 제약기업은 앞으로 일반 혁신형과 외국계 혁신형으로 구분된다. 외국계 제약기업은 두 기준 중 하나를 선택해 신청할 수 있다. 외국계 기준은 국내 연구·생산시설 유치와 해외자본 유치·공동연구 항목 배점을 높이는 대신, 기술과 특허를 본사가 보유하는 특성을 반영해 임상시험 후보물질 개발 등 일부 항목 배점을 낮췄다.
개정안은 올해 하반기 신규 인증 신청 및 인증 연장 신청부터 적용할 예정이다. 의견은 5월 6일까지 복지부 제약바이오산업과 또는 국민참여입법센터에 제출하면 된다.